Tag: magnesio
Test Salifert di durezza carbonatica e magnesio per l’acquario
Abbiamot testato i test Salifert KH e MG per misurare alcalinità e magnesio nell'acquario marino di barriera: sono economici ma validi
Smart Tester di Reef Factory per misurare in continuo Ca Mg...
Reef Factory ne ha combinata un'altra. Il nuovo Smart Tester è in dirittura d'arrivo e, per quello che ci hanno detto, è appena stato...
Soluzione ATI Analytics Reference – Lunga vita ai vostri test!
Con ATI Analytics Reference potrete verificare la validità dei vostri test ed estenderne la durata.
GHL Ion Director: ritardi e miglioramenti per la super unità di...
Miglioramenti a tutto tondo per GHL ION Director, ma purtroppo anche un leggero ritardo nei tempi di consegna, dovuti all'emergenza Coronavirus.
Come avrete intuito ci...
Reef X, Reef Y e Reef Z, i nuovi integratori di...
Amtra ha presentato allo Zoomark dello scorso anno (qui l'articolo) una nuova linea di integratori che finalmente abbiamo nelle nostre mani: Reef X, Reef...
ION Director: misurare Ca, Mg, K, Na e NO3 in automatico...
GHL ha rilasciato ION Director, un sistema che, basandosi sulla tecnologia degli ioni selettivi, riesce a misurare in automatico Ca, Mg, K, Na ed...
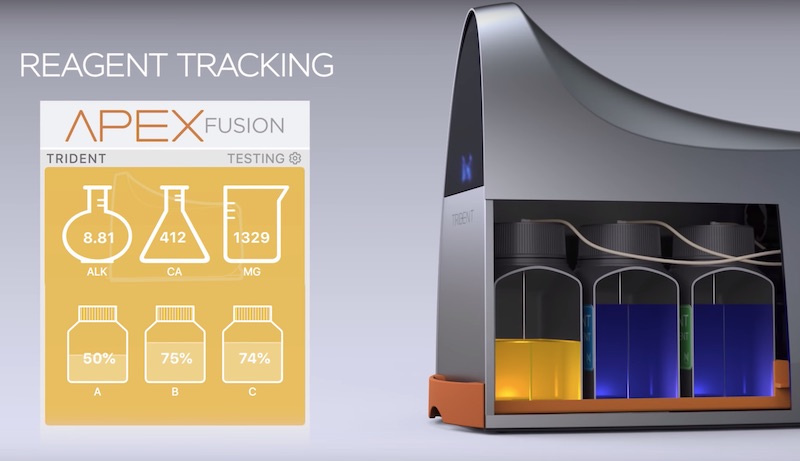
Neptune Trident: lettura automatica in acquario di calcio magnesio e kh
Ci stiamo avvicinando alla perfezione. Non possiamo descrivere meglio questo nuovo "componente" che si aggiunge alla famiglia Apex: parliamo di Neptune Trident.
L'attesa è finita...
Xepta abex e autobalance misurano in automatico ca kh k no3...
Xepta è una azienda spagnola, di Pamplona, che ha rilasciato un prodotto estremamente innovativo che può misurare in automatico in acquario Calcio, Magnesio, Potassio...
I valori ideali di inquinanti e triade nell’acquario marino di barriera
Al neofita può sembrare davvero scontato che esistano dei valori ideali e perfetti che si cerca di raggiungere in acquario. Eppure spesso leggiamo dati...
Equo presenta Vivido un promotore dell’equilibrio ecologico dell’acquario sia dolce che...
Equo Vivido è uno degli ultimi prodotti dell'azienda di Prato e si focalizza sull'equilibrio ecologico sia in ambito dolce che marino.
Equo Vivido ci è...